普众发现的核心业务模式是发现、开发及商业化ADC资产。我们的药物开发能力以从项目启动、靶点发现到临床前研究和临床开发的整个研发过程中的一体化内部能力为基础。
目前多款产品已推进至I期剂量爬坡阶段或II期剂量扩展阶段,每款产品在其靶向相同靶点的药物类别中均处于全球临床进展前列。
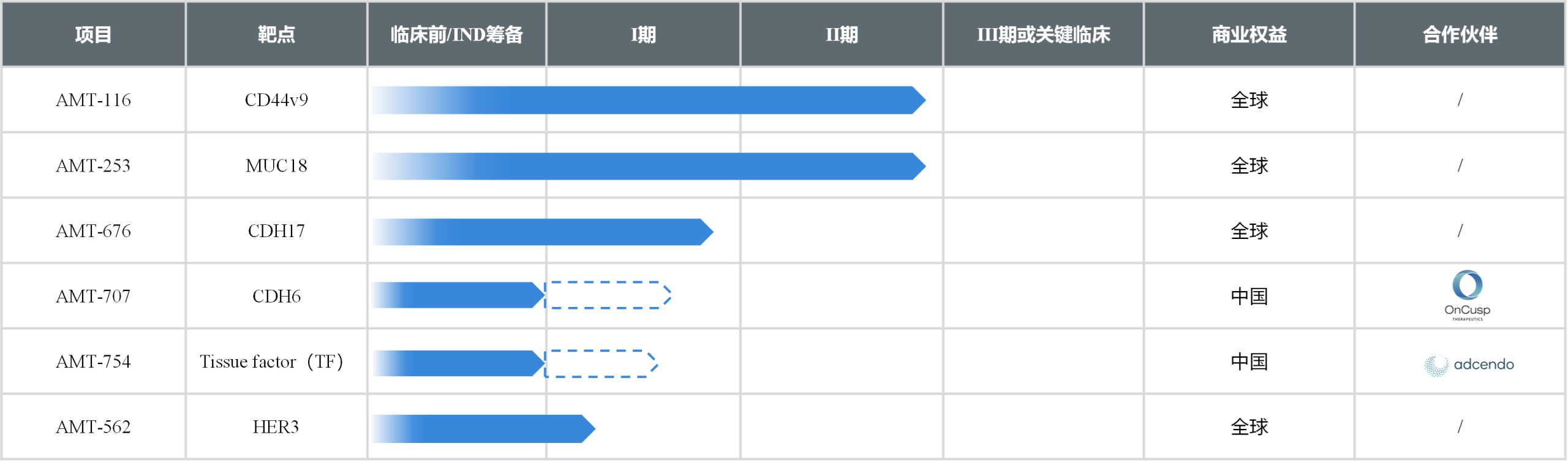
*AMT-707在美国的I期临床试验由我们的合作伙伴OnCusp Therapeutics Inc发起并进行。
**AMT-754在美国及澳大利亚的I期临床试验由我们的合作伙伴Adcendo ApS发起并进行。
管线简介
AMT-116是全球首个且唯一进入临床阶段的CD44v9靶点抗体偶联药物,为EGFR野生型非鳞状NSCLC带来具有潜力的疗效表现。CD44v9 是CD44 家族的剪接变体,属于细胞表面跨膜糖蛋白,参与细胞间及细胞-基质相互作用。其在肿瘤增殖、侵袭及治疗耐药中发挥关键作用,被公认为癌症干细胞(CSC)标志物。该靶点通过我们的MabArray靶点发现平台识别,在多种肿瘤类型中高表达,包括NSCLC、ESCC、HNSCC、NPC、三阴性乳腺癌(TNBC)及胃腺癌 (GAC)。这些特性使CD44v9 成为极具吸引力且经生物学验证的抗癌药物研发靶点。全球范围内尚无针对CD44v9 的获批药物或临床阶段药物, AMT-116成为首个且唯一进入临床探索该新型靶点的抗体偶联药物。
普众发现在2025年欧洲肿瘤内科学会(ESMO)上公布其抗CD44v9 ADC(AMT-116)用于晚期EGFR野生型非小细胞肺癌(NSCLC)及其他晚期实体瘤的初步积极数据
AMT-253是一款MUC18靶向抗体偶联药物,旨在解决黑色素瘤及妇科癌症治疗中显著的未满足医疗需求。MUC18通过我们的MabArray靶点发现平台识别,是一种在黑色素瘤细胞及肿瘤血管系统中高表达的细胞黏附分子,MUC18 是免疫球蛋白超家族的整合膜糖蛋白,在主要黑色素瘤亚型及多种其他实体瘤中高表达,而在正常组织中表达相对有限。MUC18 参与肿瘤血管生成、促进肿瘤细胞存活、增强转移及侵袭潜能,并与对若干化疗药物的耐药性相关。AMT-253是全球首款且唯一处于临床阶段的MUC18靶向抗体偶联药物。
A Cell Surface-Binding Antibody Atlas Nominates a MUC18-Directed Antibody-Drug Conjugate for Targeting Melanoma. Cancer Res. 2023;83(22):3783-3795. doi:10.1158/0008-5472.CAN-23-1356
国家药监局药品审评中心(CDE)给予普众发现AMT-253突破性治疗品种认定
普众发现在2025年欧洲肿瘤内科学会(ESMO)上公布其抗MUC18 ADC(AMT-253)用于晚期恶性黑色素瘤及其他实体瘤的初步积极数据
AMT-676是全球首款处于临床阶段的靶向CDH17的ADC,拟用于治疗结直肠癌(CRC)及其他实体瘤。CDH17是钙依赖性跨膜糖蛋白,介导肠道上皮细胞间黏附。其在多种消化道恶性肿瘤中高表达,包括结直肠癌、胃癌(GC)、胰腺癌、肝癌、食管癌及胆管癌。尽管CDH17 也在正常肠道组织中表达,但被紧密连接屏蔽,大分子药物或细胞疗法无法触及,最大限度降低潜在脱靶效应。凭借肿瘤选择性高表达、可及性及在消化道肿瘤中的广泛覆盖,CDH17成为消化道肿瘤药物研发的高潜力靶点。AMT-676是下一代消化道靶向抗体偶联药物,由新型TOP1 抑制剂有效载荷与抗CDH17 抗体偶联而成。
AMT-562是一款HER3 靶向的ADC候选药物。HER3 是EGFR酪氨酸激酶家族的独特成员,在肿瘤细胞增殖、存活及耐药性中发挥关键作用。与家族其他成员不同,HER3为假激酶,缺乏内在催化活性,需与其他 ErbB家族受体(尤其是EGFR及HER2)异源二聚化,才能激活下游PI3K/AKT及MAPK信号通路。HER3 在多种实体瘤中广泛表达,包括NSCLC、乳腺癌、结直肠癌、胰腺癌、胃癌及前列腺癌,其过表达与肿瘤侵袭性、治疗耐药性及不良预后相关。研究显示,83%的NSCLC样本及93%的CRC样本中存在HER3 表达,凸显其作为肿瘤药物开发热门治疗靶点的潜力。
AMT-562, a Novel HER3-targeting Antibody-Drug Conjugate, Demonstrates a Potential to Broaden Therapeutic Opportunities for HER3-expressing Tumors. Mol Cancer Ther. 2023;22(9):1013-1027. doi:10.1158/1535-7163.MCT-23-0198
AMT-707是一款CDH6 ADC候选药物。CDH6 是一种钙依赖性跨膜糖蛋白,属于钙黏蛋白超家族。其主要定位于上皮细胞的基底外侧膜,可介导钙依赖性细胞间黏附,并在肾脏发育中发挥关键作用。在成人正常组织中,CDH6 仅在肾脏、乳腺及胸腺中低水平表达,而在多种实体瘤(包括卵巢癌、肾癌及胆管癌)中呈显著过表达。CDH6 高表达与上皮间质转化、肿瘤侵袭及转移相关,使其成为肿瘤药物开发时具吸引力的治疗靶点。
AMT-754是一款靶向TF的ADC候选药物。TF是一种跨膜糖蛋白,作为凝血瀑布的主要启动因子发挥作用。在正常生理状态下,TF的表达局限于内皮下组织,但在多种实体瘤中存在异常过表达,包括胰腺癌、宫颈癌、食管癌、头颈部癌、卵巢癌及NSCLC。TF/FVIIa复合物的激活会促进血管生成、肿瘤生长及转移,且在多种肿瘤类型中,TF高表达均与不良临床结局相关。该等生物学特征使TF成为极具吸引力的泛肿瘤靶点。